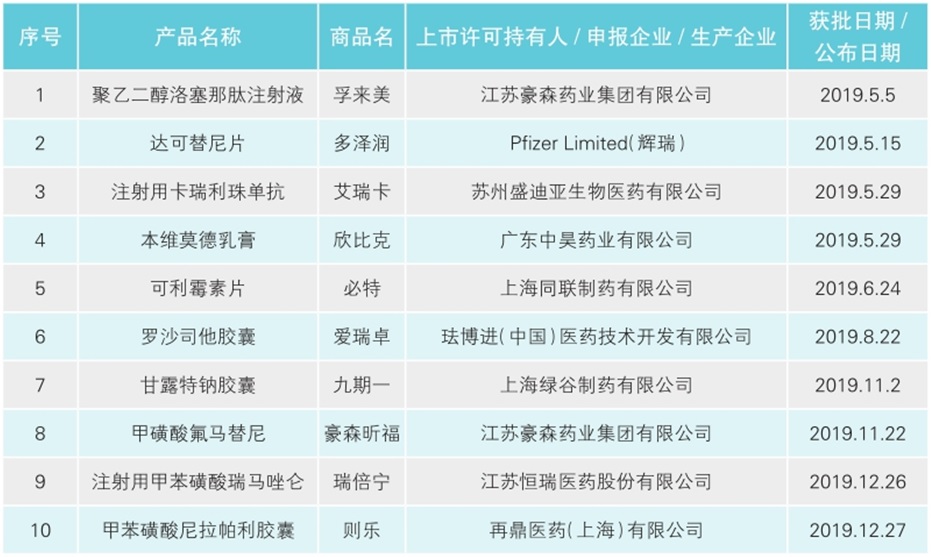
2019年,国家药监局批准了甘露特纳胶囊、本维莫德乳膏、注射用卡瑞利珠单抗等10个1类创新药,涉及糖尿病、癌症、阿尔茨海默病、感染等多个领域。
1.聚乙二醇洛塞那肽注射液(商品名:孚来美)
上市许可持有人:江苏豪森药业集团有限公司
该药是糖尿病治疗药物,2019年5月5日,国家药监局通过优先审评审批程序批准其上市。
聚乙二醇洛塞那肽不仅是我国首个自主创新的长效胰高血糖素样肽-1(GLP-1)受体激动剂,也是全球首个聚乙二醇(PEG)化的长效GLP-1受体激动剂。聚乙二醇洛塞那肽注射液可促进葡萄糖依赖的胰岛素分泌,配合饮食控制和运动,单药或与二甲双胍联合,改善成人2型糖尿病患者的血糖控制。
2.达可替尼片(商品名:多泽润)
申报企业:Pfizer Limited(辉瑞)
该药于2019年5月15日获国家药监局批准上市,可单药用于表皮生长因子受体(EGFR)19号外显子缺失突变或21号外显子L858R置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者的一线治疗。
该药的获批在我国首次实现与美国、欧洲、日本等国家和地区的同步获批。
3.注射用卡瑞利珠单抗(商品名:艾瑞卡)
生产企业:苏州盛迪亚生物医药有限公司
卡瑞利珠单抗是我国自主研发的PD-1抗体药物,可与PD-1受体结合,阻断PD-1/ PD-L1通路,恢复机体的抗肿瘤免疫力,从而形成癌症免疫治疗基础。
2019年5月29日,注射用卡瑞利珠单抗获批上市,适应症为既往接受过至少二线系统治疗的复发/难治性经典型霍奇金淋巴瘤患者的治疗。2019年9月12日,恒瑞医药(苏州盛迪亚生物医药有限公司是恒瑞医药子公司)发布公告称,国家药监局已受理卡瑞利珠单抗单药二线治疗晚期食管鳞癌、卡瑞利珠单抗联合培美曲塞加卡铂一线治疗晚期或转移性非鳞状非小细胞肺癌的上市申请。
4.本维莫德乳膏(商品名:欣比克)
上市许可持有人:广东中昊药业有限公司
该药是我国自主研发的1类新药,用于局部治疗成人轻至中度稳定性寻常型银屑病,经优先审评审批程序,于2019年5月29日获国家药监局批准上市。
本维莫德是一种酪氨酸蛋白激酶抑制剂,该药的上市将为银屑病患者提供一种新的药物治疗手段。
5.可利霉素片(商品名:必特)
生产企业:上海同联制药有限公司
可利霉素是一种治疗细菌感染的大环内酯类抗生素,该药为国内第一个具有自主知识产权的抗生素类1.1类新药,于2019年6月24日获批上市。
可利霉素由中国医学科学院医药生物技术研究所采用“合成生物学技术”研发,后与沈阳同联制药集团合作开发。该药由中国医学科学院医药生物技术研究所、沈阳同联制药集团和北京首科集团共同申报。
6.罗沙司他胶囊(商品名:爱瑞卓)
上市许可持有人:珐博进(中国)医药技术开发有限公司
该药由阿斯利康与珐博进合作开发,是全球首个开发的小分子低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)类治疗肾性贫血的药物。罗沙司他也是首个中国本土孵化、首个率先在中国获批的全球首创原研药,2018年底获国家药监局批准上市,用于治疗正在接受透析治疗的患者因慢性肾脏病(CKD)引起的贫血。
2019年8月22日,阿斯利康宣布该药新适应症上市申请获国家药监局批准,适用于非透析依赖性慢性肾病(NDD CKD)的贫血治疗。
7.甘露特钠胶囊(商品名:九期一)
上市许可持有人:上海绿谷制药有限公司
甘露特钠胶囊(有效成分:甘露寡糖二酸)由上海药物研究所、中国海洋大学和上海绿谷制药联合开发。该药是我国拥有自主知识产权的创新药,获得国家“重大新药创制”科技重大专项支持。
2019年11月2日,国家药监局有条件批准九期一上市,用于治疗轻度至中度阿尔茨海默病,改善患者认知功能。国家药监局要求该药上市许可持有人继续进行药理机制方面研究和长期安全性有效性研究,完善寡糖的分析方法,按时提交有关试验数据。
8.甲磺酸氟马替尼(商品名:豪森昕福)
上市许可持有人:江苏豪森药业集团有限公司
该药是我国拥有自主知识产权的创新药,用于治疗费城染色体阳性的慢性髓性白血病(Ph+CML)慢性期成人患者,于2019年11月22日通过优先审评审批程序获批上市。
该药在第一代酪氨酸激酶抑制剂(TKI)伊马替尼分子结构基础上进行了优化设计和修饰,疗效和安全性得到“双向优化”。
9.注射用甲苯磺酸瑞马唑仑(商品名:瑞倍宁)
申报企业:江苏恒瑞医药股份有限公司
瑞马唑仑由Paion AG公司开发,用于手术中的全身麻醉。甲苯磺酸瑞马唑仑是瑞马唑仑的改盐化合物。
2019年12月26日,注射用甲苯磺酸瑞马唑仑获批上市,用于常规胃镜检查的镇静。该药是我国自主研发并拥有自主知识产权的创新药。
10.甲苯磺酸尼拉帕利胶囊(商品名:则乐)
上市许可持有人:再鼎医药(上海)有限公司
2019年12月27日,国家药监局通过优先审评审批程序附条件批准该药上市,用于铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。
由于该药是附条件批准,国家药监局要求药品上市许可持有人在产品上市后继续按计划完成正在开展的临床研究。
